硫酸還元バクテリアの硫黄同位体分別
海底堆積物中の硫化物の硫黄同位体比。
| |||||||||||||||||||||||||||||||||||||||||||||||
硫酸還元バクテリアの硫黄同位体分別の大きさは、硫酸還元速度や環境温度の影響を受ける。これらの効果をどのように評価するかで、先カンブリア時代の堆積岩の硫黄同位体比の意味が大きく違ってくる。
1960年代に世界各地の海底堆積物中の硫化物の硫黄同位体比が測定された。その結果、堆積物中の硫化物の硫黄同位体比は海水の硫黄同位体比(+20‰)に比べ、40~60‰軽い同位体組成をもっていた。
文献
実験室における硫酸還元バクテリアの硫黄同位体比分別
ところが室内実験で硫酸還元バクテリアを培養し、硫黄同位体の分別量を測定すると、4~20‰の範囲となり、天然における硫黄同位体分別に比べて小さいことが問題になった。
Kaplan and Rittenberg (1964)は、栄養塩の種類、温度、硫酸濃度を変えて実験し、次のような結果を得た:
- 還元速度は、濃度20~60 μmol∕Lの範囲では、硫酸濃度に影響されない。
- 還元速度は電子供与体の種類に依存し、水素、乳酸塩、エタノールの順に急速に減少する。
- 還元速度は、絶対温度に逆比例して大きくなる。
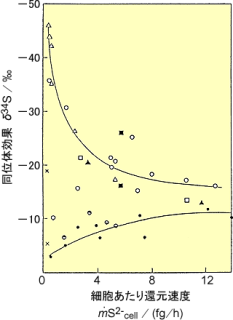
一方、同位体分別については、硫酸還元速度と同位体効果の関係を図示している。
硫酸還元細菌デスルフォヴィブリオ(Desulfovibrio desulfuricans)の休止セルによる硫酸還元速度と同位体効果の関係。
温度: 10~45℃
縦軸: 実験開始時の硫酸のδ34S - 発生した硫化水素のδ34S
酒井; 松久 1996 安定同位体地球化学. 71. 図3‐7. from Kaplan; Rittenberg. 1964
|
この図で還元速度が小さい領域で、-46‰に達する大きな同位体効果が認められたことは、新たな問題を発生させた。ソードの遷移状態理論によって求められた最大同位体効果-35‰より大きな同位体効果を越えていたのである。これを説明するために、硫酸還元バクテリアの定常状態モデルが提示された。
文献
Kaplan, IR; Rittenberg, SC. 1964. Microbiological fractionation of sulphur isotopes. Journal of General Microbiology, 34, 195–212.